在新药研发的漫长过程中,实验动物模型是药物从临床前试验阶段进入到临床试验阶段的金标准。实验动物模型有助于人们了解疾病的起源、病理生理特征、疾病机制、识别药物靶标、评估新药物的疗效和人体毒性以及进行药代动力学评价等。常用的实验动物模型包括小鼠、大鼠、兔子、犬、猴等,这些动物模型在推进人类药物研究进展中做出了重大贡献。

然而,实验动物模型也存在一定局限性
首先,昂贵的动物模型增加药物研发的成本
辄成千上万的实验动物令许多研究者望而却步,实验动物的长生长周期也拉长了研发的时间线。药物研发的高失败率和动物实验数据的必要性极大提高了药物研发企业的研发成本。
其次,动物模型实验的进行常常伴随着伦理争议
在进行生命科学的研究时,研究人员必须爱护实验动物,正确对待实验动物生命,维护实验动物的福利伦理。随着社会的发展,实验设计中的动物伦理问题越来越引起人们的关注。
最后,实验动物由于自身生理复杂性和与人类的物种差异,在临床前的药物疗效和毒性评估准确性上也会有所折扣
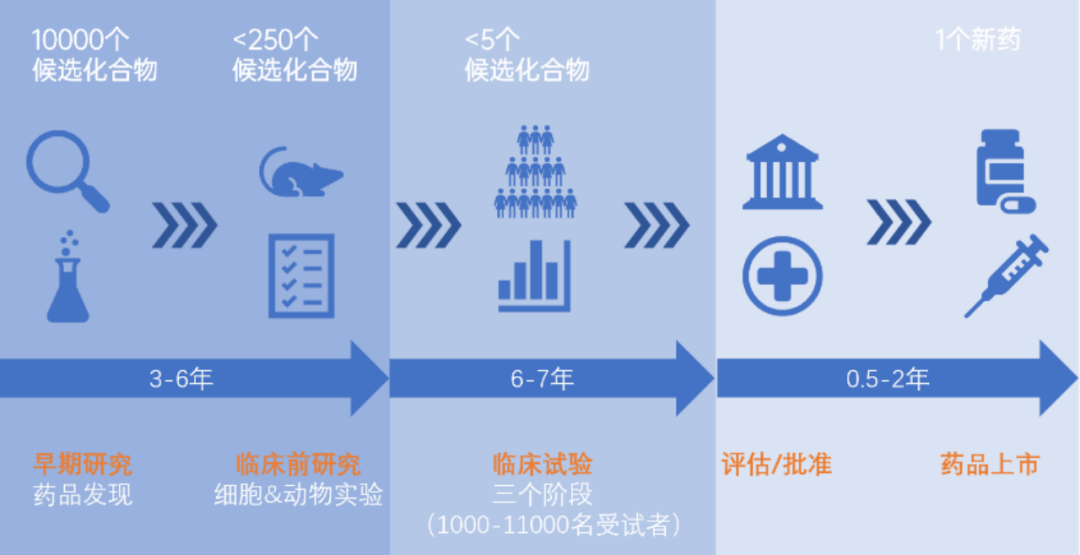
有研究表明,现行动物模型在预测新药毒性上仅有约70%的准确性。由于这种不确定性,大约40%的新开发药物即使通过了动物模型的临床前评估最终也会在临床试验阶段折戟。因此,人们迫切需要仿生人体病理生理学的替代模型来弥合动物模型与人体临床试验之间的差距。
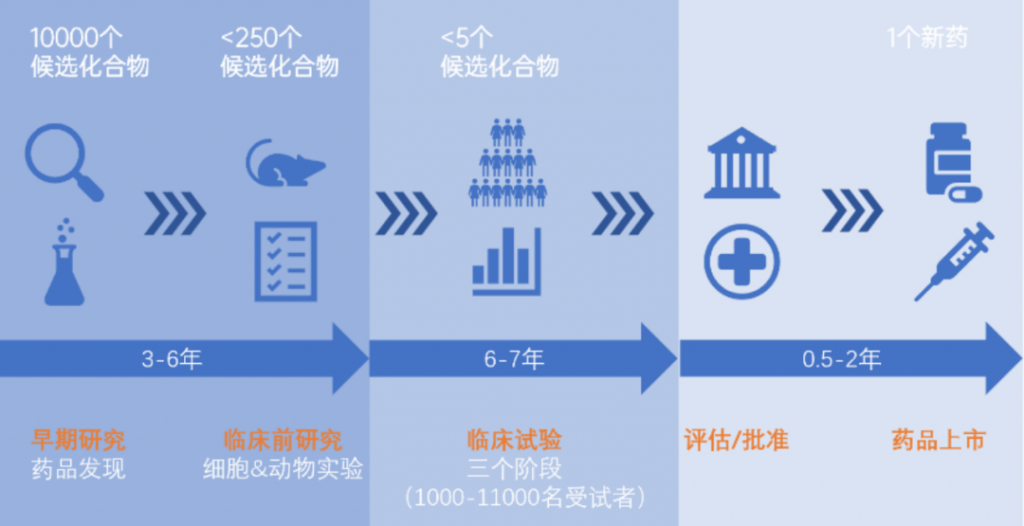
器官芯片的诞生,有望改善这一现状,甚至将传统实验动物从实验室“解救”出来。器官芯片是一种在微米纳米尺度上的包含可连续灌流腔室的三维细胞培养装置。2011年,来自哈佛大学Wyss研究所的Donald Ingber教授研究团队在《Science》杂志上率先发表了利用PDMS制造的标志性体外肺芯片,通过将人肺泡上皮细胞和微血管内皮细胞引入各自的通道,在体外构建了仿生肺芯片模型。随后,越来越多的人体器官芯片被开发出来,如肝脏芯片、肾脏芯片、胰脏芯片、心脏芯片、肠芯片、血脑屏障芯片及骨骼和骨髓芯片等,这些芯片被成功应用于疾病机制研究和药物不良反应分析等。近年来,集成多器官单元的多器官芯片也开始引起人们的关注,如利用肠、肝、皮肤和肾依次连接的四器官芯片用于测试候选药物的全身毒性及药代动力学和药效学分析等。

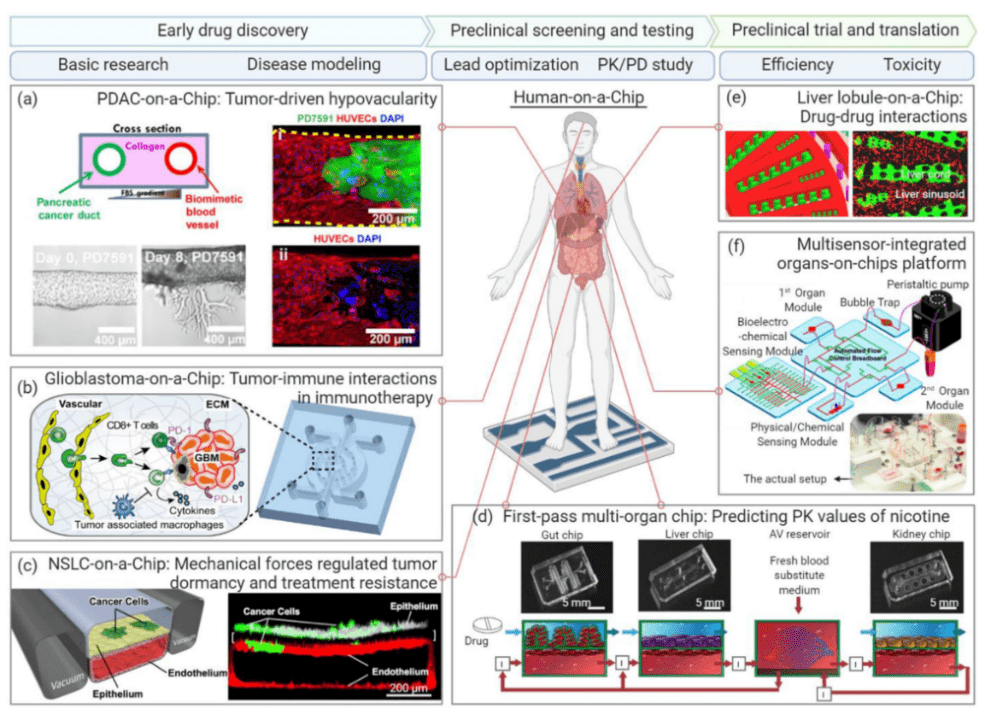
在早期药物研究中,器官芯片可有助于提高人类对疾病的基本生理病理学和潜在机制的认识。器官芯片在体外构建出的疾病模型可以揭示关键的病理机制,并确定改善治疗结果的生物标志物和靶点。在临床前筛选和测试中,由代谢相关器官组成的多器官芯片系统很适合在不同器官和不同给药条件下进行药代动力学和药效学研究。在药物安全性和有效性评价方面,器官芯片可以作为准确评估药物毒性的有用工具。另外,器官芯片在个性化治疗上也具有巨大的潜力,利用特定患者供体的原代细胞,可以在病理生理环境中评估患者特异性的药物反应。


-300x128.jpg)
-300x128.jpg)